No hay duda de que podemos afirmar que la investigación constituye una actividad que interesa, tanto a los pacientes, como a los profesionales sanitarios:
- mejora la calidad asistencial,
- disminuye su variabilidad
- mejora el principio de equidad
- forma parte de lo que el profesional debe hacer
- reporta beneficios al profesional (mejora la formación, aumenta la motivación y la satisfacción profesional)
- debe ser garantizada por los gestores y planificadores (aporta a los servicios de salud calidad, efectividad y eficiencia)
La información clínica almacenada en registros de diverso tipo constituye una herramienta fundamental para la investigación. ´
Hasta hace pocos años, el acceso a la información clínica y/o administrativa de los pacientes con fines de investigación apenas tenía limitaciones.
Sin embargo, con la legislación vigente en materia de protección de datos de carácter personal y documentación clínica, esta situación se ha modificado, al existir importantes restricciones a su acceso.
Así mismo, la petición de consentimiento informado a los participantes del estudio puede introducir sesgos de selección.
Por lo tanto, nos encontramos en una situación que dificulta la investigación, lo que podría llegar a limitar considerablemente el avance del conocimiento, obstaculizar las posibilidades de formación de profesionales sanitarios, y disminuir la calidad y eficiencia de la atención que se presta.
El uso de los datos de carácter personal con fines de investigación está legitimado por nuestra legislación, sin embargo, esta información debe ser tratada de forma confidencial en todo momento.
La legislación ofrece dos alternativas:
- el consentimiento del paciente
- el tratamiento disociado de la información.
Sin embargo, en algunos supuestos, resulta realmente difícil el cumplimiento de las exigencias legales, planteándose preguntas del tipo:
- ¿a quién se considera facultativo directamente implicado en el diagnóstico y tratamiento del enfermo en un centro de salud?
- cuando un facultativo quiere investigar con pacientes que no son de su cupo, ¿cómo accede a los datos de estos pacientes?
- en este caso, ¿quién puede acceder previamente a la información en su integridad para someterla al procedimiento de disociación para obtener los datos?
- ¿cómo obtener los datos personales de un paciente para conseguir su consentimiento?
- ¿qué hacer cuando no es posible obtener el consentimiento de los pacientes y los datos no se pueden disociar?
Como vemos, en algunos supuestos, el cumplimiento de las exigencias legales a la hora de obtener datos para investigar se hace realmente difícil, planteándose una serie de dificultades que en muchos casos imposibilita el desarrollo de la investigación.
En este post marcaremos una orientación sobre el acceso a la información contenida en registros, respetando los derechos de los pacientes y la legislación vigente.
Revisaremos distintos supuestos para definir un posible procedimiento de actuación que nos oriente sobre el acceso a la información contenida en registros informatizados y no informatizados (historia clínica, bases de datos, tarjeta sanitaria) respetando los derechos de los pacientes y la legislación vigente.

NORMATIVA
A nivel nacional, la aprobación de la Ley Orgánica 3/2018, de Protección de Datos y Garantía de los Derechos Digitales ha abierto nuevas vías al tratamiento de datos con fines científicos y de investigación.
Así, su Disposición Adicional Decimoséptima, sobre tratamientos de datos de salud, ha definido un nuevo marco en España para la investigación científica.
Esta norma incorpora previsiones de significado particularmente relevante para la investigación en salud como la pseudonimización -técnica de amplio uso en la investigación sanitaria-, y las cuestiones planteadas por la anonimización, por la protección de datos personales desde el diseño y por defecto, así como por el análisis de impacto en la protección de datos.
La comunicación oral o escrita, la presentación de casos clínicos y series de casos y el tratamiento de imágenes que hacen referencia al paciente, constituyen actividades de investigación o científicas que suponen un tratamiento de los datos personales del paciente, por lo que su ejecución se encuentra sometida a los principios que establece la legislación vigente en materia de protección de datos.
Para analizar en qué condiciones debe efectuarse ese tratamiento de datos, debe estudiarse el cumplimiento de cada uno de los principios que el RGPD establece para el uso de los datos que hacen referencia a una persona, haciendo especial incidencia en el de legitimidad de la finalidad perseguida y en el requerimiento de contar con consentimiento del interesado para poder tratar sus datos personales.
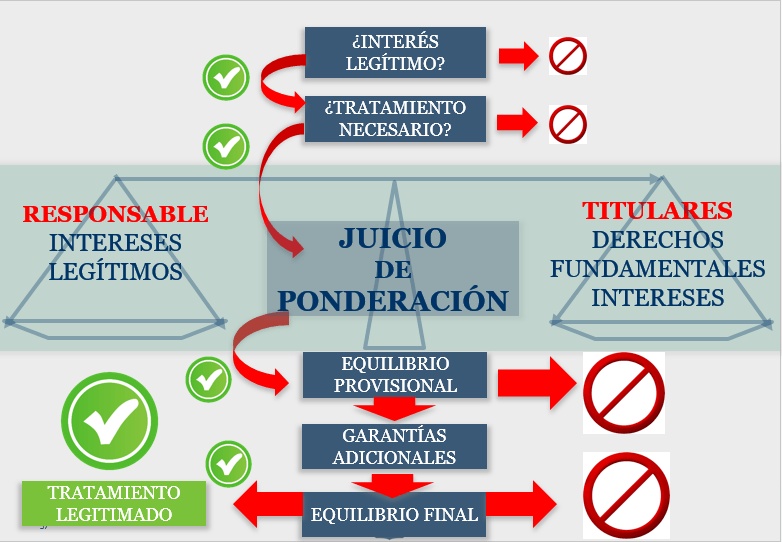
LEGITIMACIÓN DE LA FINALIDAD
La Ley General de Sanidad, establece en su artículo 6 que las actuaciones de las Administraciones Públicas Sanitarias estarán orientadas, entre otros supuestos, a:
«garantizar que cuantas acciones sanitarias se desarrollen estén dirigidas a la prevención de las enfermedades y no sólo a la curación de las mismas».
Además, su artículo 18 indica como una de las actuaciones sanitarias del Sistema de Salud:
«el fomento de la investigación científica en el campo específico de los problemas de salud».
La misma Ley, establece en su artículo 61 que:
«… la información relativa a cada paciente … estará a disposición de los enfermos y de los facultativos que directamente estén implicados en el diagnóstico y el tratamiento del enfermo, así como a efectos de inspección médica o para fines científicos, debiendo quedar plenamente garantizados el derecho del enfermo a su intimidad personal y familiar y el deber de guardar el secreto por quien, en virtud de sus competencias, tenga acceso a la historia clínica.
Los poderes públicos adoptarán las medidas precisas para garantizar dichos derechos y deberes», y en su artículo 68, que:
«los centros hospitalarios desarrollarán, además de las tareas estrictamente asistenciales, funciones de promoción de salud, prevención de las enfermedades e investigación y docencia, de acuerdo con los programas de cada Área de Salud, con objeto de complementar sus actividades con las desarrolladas por la red de Atención Primaria».
Por su parte, la nueva ley básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica, establece los siguientes principios; su artículo 2:
«la dignidad de la persona humana, el respeto a la autonomía de su voluntad y a su intimidad orientarán toda la actividad encaminada a obtener, utilizar, archivar, custodiar y transmitir la información y documentación clínica»;
su artículo 7:
«toda persona tiene derecho a que se respete el carácter confidencial de los datos referentes a su salud, y a que nadie pueda acceder a ellos sin previa autorización amparada por la ley».
y su artículo 16:
«el acceso a la historia clínica con fines judiciales, epidemiológicos, de salud pública, de investigación o de docencia, se rige por lo dispuesto en la normativa, de Protección de Datos de carácter personal, y en la Ley General de Sanidad, y demás normas de aplicación en cada caso».
En conclusión, la Ley considera, como no podría ser de otra forma, que la docencia y la investigación constituyen dos actividades necesarias para el desarrollo de las actuaciones sanitarias que se atribuyen al Sistema de Salud, pero garantizando, en todo caso, el derecho del enfermo a su intimidad personal y familiar.

CONSENTIMIENTO DEL AFECTADO
En el caso que nos ocupa, cualquier actividad de investigación o docencia desarrollada con los datos de un paciente obtenidos en la actividad asistencial debe tenerse en cuenta que estamos utilizando datos obtenidos del paciente para una finalidad muy concreta, su atención sanitaria y en unas determinadas condiciones, a un uso completamente diferente como es el de investigación o docencia, del cual no se ha informado expresamente al ciudadano y para el que no hemos recabado, en el normal de los supuestos, su consentimiento, y que aunque la normativa considere como actividad no incompatible, debe ajustarse al principio de consentimiento previo que establece la normativa sobre Protección de Datos Personales.
La Ley básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica, establece en su artículo 16.1 que
«el acceso a la historia clínica con estos fines (de investigación o docencia) obliga a preservar los datos de identificación personal del paciente, separados de los de carácter clínico-asistencial, de manera que como regla general quede asegurado el anonimato, salvo que el propio paciente haya dado su consentimiento para no separarlos».
Con ello, se abren dos posibles vías o modos de realizar estos trabajos:
- con datos disociados, cuando no sea posible asociarlos con una persona concreta
- con datos en los que aparece identificado de forma inequívoca el titular de esa información.
- Con datos disociados
Con datos disociados
En el supuesto de disociación, la Ley establece el criterio de que la persona que pretenda acceder a los datos con fines científicos, no tenga acceso en ningún caso a aquellos datos que identifican al titular de los mismos.
Esta tarea debe haberse realizado con carácter previo al acceso de los datos, de tal manera que la forma de almacenamiento de la documentación clínica distinga entre los datos identificativos y los clínico-asistenciales que figurarán en ficheros anónimos y que sólo el personal encargado de gestionar los archivos pueda relacionar cuando sea necesario.
Cuando los datos que se utilicen respondan a estas características y sea imposible saber a quién corresponden los datos que se tratan, el tratamiento queda excluido del ámbito de aplicación de la normativa en materia de Protección de Datos (LOPD).
Con datos en los que aparece identificado de forma inequívoca el titular de esa información.
Cuando el tratamiento de los datos requiera conocer a quién corresponden, utilizando para ello los datos identificativos, será necesario el consentimiento inequívoco para tratar los datos del paciente con fines de investigación o docencia, circunstancia que se producirá cuando se cumpla la obligación de información previa que contempla la normativa sobre Protección de Datos.
Con carácter previo a la recogida de la información se debe informar al ciudadano de quién es el responsable de los datos que se están recabando y cuál es la finalidad a la que se van a destinar.
Sólo cuando se cumpla este principio de información estaremos legitimados para poder realizar el tratamiento de los datos.
Además, debe tenerse en cuenta que el consentimiento del interesado es revocable en cualquier momento y por cualquier causa, teniendo el titular de los datos la plena disponibilidad sobre los mismos.
También debe tenerse en cuenta que al tratarse de datos especialmente protegidos, tal y como los califica la normativa sobre Protección de Datos, el consentimiento necesario tiene que tener la característica de ser expreso, no siendo suficiente en ningún caso cualquier tipo de consentimiento presunto o tácito.
Para poder tratar datos referentes a la salud de las personas para fines distintos a los propiamente asistenciales, requeriremos una manifestación clara e inequívoca de voluntad del paciente que nos autorice a realizar el tratamiento de datos que pretendemos.

CONSIDERACIONES PREVIAS
La investigación que se realiza utilizando registros debe estar bien fundamentada y desarrollarse con una metodología correcta.
La primera norma ética que se debe valorar en un trabajo de investigación es su corrección técnica.
Sin ella, la investigación carece de justificación, ya que no será capaz de alcanzar los objetivos que se plantea.
Ello se basa en que la relación beneficio/riesgo para los participantes debe ser siempre favorable.
Si por ser incorrecta la metodología, el conocimiento obtenido es nulo o erróneo, cualquier riesgo asumido será gratuito y por tanto inadmisible.
Todo trabajo de investigación se deberá sustentar en un protocolo con los siguientes apartados:
- justificación,
- objetivos,
- variables a recoger,
- metodología de recogida de datos,
- fuentes de información,
- consentimiento informado (si es posible obtenerlo),
- compromiso del investigador de respetar el protocolo y la confidencialidad
- y conformidad de los colaboradores.
La información que se debe recoger de los sujetos debe ser consistente con los objetivos del estudio.
Se deben sopesar los datos que se recogen, principalmente cuando se refieren a información especialmente sensible (adicción a drogas, orientación sexual, etc.).
Otro aspecto a valorar es que el conocimiento obtenido de la investigación deberá resultar útil, al menos, para la población de la que proceden los sujetos sometidos a la investigación.
Estas consideraciones han de ser valoradas de forma independiente del investigador o institución que realice la investigación.
Es decir, han de ser evaluadas por un Comité de Ética de la Investigación (CEI), que valorando el riesgo potencial de la investigación (principalmente derivado de la intromisión en la esfera de la privacidad o intimidad de los pacientes) establecerá los requisitos necesarios para que se pueda garantizar el respeto a los derechos humanos y la observación de los principios éticos básicos.
Acceso a datos clínicos y/o administrativos. Situaciones posibles
Contemplamos diferentes situaciones relativas a la utilización de datos clínicos y administrativos.
Acceso a datos anonimizados
Las colecciones de datos anónimos y los registros anonimizados pueden ser utilizados y cedidos sin el consentimiento informado de los sujetos.
Estos datos son un tipo de información cuyo tratamiento queda fuera de los requerimientos establecidos por la normativa de protección de datos de carácter personal.
Este supuesto no precisaría de especiales consideraciones éticas, al no poder asociarse la información con persona alguna.
De hecho, son varias las recomendaciones que lo clasifican dentro de la investigación «no clínica».
Acceso a datos no anonimizados. Datos administrativos de usuarios de un área de salud
La utilización de los datos administrativos es posible, siempre que se obtengan para contactar con los titulares, al objeto de obtener su consentimiento. para participar en cualquier actividad investigadora.
No obstante, se deberían cumplir una serie de requisitos:
- Se precisará de la autorización del responsable del fichero. Sólo el responsable del fichero está legitimado para usar los datos para contactar con sus titulares al objeto de obtener su consentimiento para participar en una investigación.
- El fichero con los datos personales de los usuarios se deberá entregar al investigador principal o persona responsable de la investigación preservando la seguridad de acceso a los mismos.
- En caso de que sea necesario contactar con el titular de los datos, a través de una carta para pedirle la participación en el estudio, ésta irá firmada por el órgano competente y el investigador. Si el contacto se realiza por teléfono, será necesario un compromiso de confidencialidad por parte de la persona que realiza las llamadas.
No es posible ceder los datos a un tercero para que sea éste el que los utilice para contactar con los interesados, salvo que se haga mediando un contrato de encargo de tratamiento, realizando el trabajo en nombre y por encargo de la institución sanitaria pública, que deberá ser previamente informado por la agencia de protección de datos antes de su firma.
En el caso de los menores de 13 años se pueden obtener los datos de identidad y dirección del padre, madre o tutor del registro correspondiente con la única finalidad de recabar la autorización para requerir el consentimiento de los padres o tutores.
Datos contenidos en la historia clínica
Como norma general, siempre que haya que acceder a datos contenidos en las historias clínicas, se realizará un proceso de anonimización que permita obtener los datos clínicos de interés, separándolos de los identificativos (por ejemplo, utilizando procedimientos informáticos para la extracción selectiva de estos datos).
Cuando esto no sea posible, será necesario que el investigador solicite el consentimiento informado de los sujetos, de acuerdo con la legislación vigente.
En relación al consentimiento informado, hay que tener en cuenta que es un proceso que requiere información, comprensión y voluntariedad.
- Hay que informar al interesado, de forma expresa y clara de cuál es la finalidad que se persigue (para qué van a utilizarse los datos), así como de quiénes van a tener acceso a los mismos (especialmente en el caso de que vayan a ser cedidos a terceros para que realicen la actividad de investigación) y de la posibilidad de revocar el consentimiento en cualquier momento, así como de los derechos que la normativa de protección de datos les reconoce (acceso, rectificación, oposición a un uso posterior, supresión, limitación del tratamiento, portabilidad de los datos, y a no ser objeto de decisiones individuales automatizadas).
- Si se utilizan datos de carácter personal en menores de edad o incapaces, deberá justificarse científicamente la necesidad de incluir a dichas poblaciones en la investigación. Será necesario el consentimiento de los padres o representantes legales. En estos casos, se debe garantizar que el riesgo de la investigación es inexistente o mínimo, y que los conocimientos que así se obtienen no pueden obtenerse de otro modo.
Posibles situaciones
-no es posible obtener el consentimiento informado.
Puede haber situaciones en las que es prácticamente imposible obtener el consentimiento de cada una de las personas que integran el estudio, por falta de recursos materiales o humanos, o por imposibilidad de contactar con los sujetos.
En estos casos, la alternativa que nos plantea la legislación para cumplir las exigencias legales es el tratamiento disociado de la información, es decir, manejar datos anonimizados.
Sin embargo, para llevar a cabo esta disociación hay un paso previo que plantea cierta problemática:
¿qué profesional está autorizado para acceder, revisar y extraer los datos de la historia clínica del paciente para posteriormente anonimizarlos?
Ante esto se pueden plantear dos supuestos distintos:
•Pacientes pertenecientes al mismo centro que los investigadores:
Según la LGS, la información de cada paciente estará a disposición de los facultativos que directamente estén implicados en el diagnóstico y el tratamiento del enfermo, así como para fines científicos.
En nuestro sistema sanitario, todos los médicos de un centro de salud pueden acceder, con fines asistenciales, a las historias de los pacientes adscritos a dicho centro, ya que son parte del equipo médico que puede atender a cualquier paciente del centro (urgencias/suplencias/doblajes).
Cuando se accede a los datos de la historia clínica con fines de investigación, los profesionales sanitarios y el personal que accede en el ejercicio de sus funciones (siendo una de ellas la investigación) queda sujeto al deber de secreto profesional (artículo 16.6 de la Ley 41/2002) no pudiendo revelar los datos a un tercero.
En estos casos, la obtención de la información se realizaría desde el mismo centro, utilizando las claves de los investigadores para el acceso habitual a las historias clínicas.
Una vez extraída la información necesaria, se deberá someter a un proceso de disociación de manera que la identidad del sujeto quede desligada de los datos de carácter personal o su asociación no esté al alcance del investigador.
•Pacientes pertenecientes a un centro distinto al de los investigadores:
Si los investigadores no forman parte del equipo médico que atiende o puede atender a los pacientes, se podría acceder a dicha información mediante la extracción de datos realizada por el equipo médico del sujeto, incorporando posteriormente un procedimiento de disociación adecuado, antes de ceder la información a los investigadores.
Se podría plantear una excepción en caso de imposibilidad de la colaboración del equipo médico habitual de los pacientes y ausencia de riesgo de uso indebido de la información.
En este caso, para la obtención de la información por parte de investigadores ajenos al centro, cobra especial interés el informe de un CEI que valore los aspectos éticos y la necesidad e importancia del proyecto.
El estudio debe considerarse de indudable interés para la salud pública y el riesgo para el sujeto de investigación (incluyendo el riesgo de vulnerar la confidencialidad de sus datos), que debe ser mínimo.
-No es posible anonimizar los datos personales ni obtener el consentimiento informado
Otra situación que se da con cierta frecuencia, tanto si los pacientes pertenecen al mismo centro que los investigadores como si no, es el caso de proyectos en los que, en una primera fase del estudio, no es posible anonimizar los datos personales o clínicos de los sujetos, ni tampoco obtener el consentimiento informado para ello.
Supongamos que la población objeto del estudio de investigación son sujetos con una determinada condición clínica o enfermedad.
Para ello es necesario obtener listados de pacientes con esta enfermedad de los que extraer una muestra de sujetos (por ejemplo, pasar una encuesta de calidad de vida a pacientes con cardiopatía isquémica, contactar con adolescentes que han sufrido una interrupción voluntaria del embarazo, etc.).
De esta forma, los listados de pacientes no pueden estar anonimizados, y sólo se podría obtener el consentimiento informado a posteriori, tras contactar con ellos.
En estos casos el profesional encargado de obtener estos listados debe garantizar en todo momento la confidencialidad de estos datos, por lo que el fichero con los datos personales de los usuarios se deberá entregar al investigador principal o persona responsable de la investigación preservando la seguridad de acceso a los mismos e, igualmente que en el apartado anterior, será imprescindible la valoración de un CEI.

CONCLUSIÓN
Hemos intentado recopilar algunos de los supuestos más comunes que se presentan a la hora de desarrollar un proyecto de investigación.
Probablemente, con el marco legal actual, quedan otras situaciones que no hemos contemplado y que, si se analizan, siguen planteando multitud de dudas.
Siempre con carácter de excepcionalidad, podemos realizar una consideración ética relativa a limitar la intimidad de las personas para permitir una actividad investigadora en beneficio de la comunidad.
Es especialmente importante el principio de la necesidad y proporcionalidad en el tratamiento de datos personales.
Para valorar la necesidad, nos plantearemos si el mismo fin (el estudio epidemiológico o de investigación) no pueda ser desarrollado sin datos de carácter personal.
En relación con la proporcionalidad, valoraremos que el fin a alcanzar (la actividad epidemiológica o de investigación) es proporcional con el medio (el tratamiento de los datos de salud).
En esta situación, pueden ser de utilidad las directrices del Medical Research Council sobre el manejo de información clínica en la investigación médica a la hora de hacer una excepción al consentimiento.
Y, al igual que planteábamos anteriormente, cobra especial importancia el informe de un CEI, que valore los aspectos éticos y la necesidad e importancia del proyecto como de indudable interés para la salud pública.
Directrices del Medical Research Council sobre manejo de información clínica en la investigación médica
| Necesidad | ¿Hay alternativas válidas para hacer el estudio? ¿Se podría utilizar información anonimizada? |
| Sensibilidad | ¿Qué y cuán sensible es la información que requiere la investigación? |
| Importancia | ¿Contribuirá la investigación a incrementar el conocimiento de una manera sustantiva? |
| Salvaguardas | ¿Están previstas las medidas de seguridad para impedir filtraciones y evitar daño a los pacientes? |
| Revisión independiente | ¿Ha evaluado un comité de ética de la investigación la propuesta y respalda la excepción? |
Esperamos que la anterior información le haya resultado de utilidad.





